Биофильтр для искусственного водоёма
Биологическая фильтрация.
Под биологической фильтрацией понимается бактериальное превращение органических азотистых соединений в нитраты.
Стадии этого процесса известны под общим названием "азотный цикл". Хотя азотный цикл начинается с превращения азотсодержащих органических соединенинй в аммиак, желательно, чтобы первая стадия уже закочилась, прежде чем материал поступит на биологический фильтр. Основным назначением биологического фильтра является превращение аммиака в нитриты, а нитритов в нитраты. Эти реакции имеют большое значение, когда искусственный водоём заселен рыбой, поскольку аммиак - высокотоксичный продукт обмена, непосредственно выделяемый многими водными организмами, и побочный продукт жизнедеятельности многих бактерий. Нитриты несколько менее токсичны, чем аммиак в форме NH3, хотя для некоторых видов и они токсичны в концентрациях менее 2.5 мг/л. Нитраты для большинства водных организмов считаются относительно нетоксичными.
Устройство биологического фильтра для искусственного водоёма.
Биологический фильтр обычно представляет собой пористый твердый слой, в котором содержатся нитрифицирующие бактерии. Бактерии извлекают необходимые им питательные вещества и кислород из воды, протекающей через фильтрующий слой. Простой биологический фильтр представляет собой ящик, наполненный гравием. Вода поступает сверху, протекает через фильтующий слой и вытекает через дренажные трубы на дне ящика.

Рис. 1. Простой нисходящий биологический фильтр.
Существует несколько типов биологических фильтров:
- Погружные фильтры (типа фильтра, показанного на рис. 1) - это фильтры, у которых фильтрующий слой полностью погружен в воду. Погружные фильтры подразделяются на нисходящие и восходящие в зависимости от направления тока воды. В нисходящем фильтре вода поступает сверху и вытекает снизу, а в восходящем фильтре поток воды направлен снизу вверх. Иногда применяют также погружные фильтры с горизонтальным током воды.
- Капельные фильтры - это биологические фильтры, в которых уровень воды поддерживается ниже дна фильтра. Вода поступает сверху и образует водяную пленку на поверхности твердой фазы, но не заполняет пор между частицами фильтрующего слоя. Это обеспечивает нисходящий поток воды и естественную аэрацию в результате прохождения воздуха через фильтр.
Наиболее эффективными являются восходящие погружные и капельные фильтры. В капельных фильтрах поступление кислорода обеспечивается естественной конвекцией воздуха, и фильтры засоряются твердыми веществами. Однако продолжительность удерживания можно регулировать только путем увеличения толщины фильтрующего слоя. Восходящие затопленные фильтры меньше других погружных фильтров засоряются твердыми веществами. Они позволяют также регулировать продолжительность удерживания в широком диапазоне путем изменения скорости протекания воды.
Процессы, проходящие в биологическом фильтре для искусственного водоёма.
Нитрификация является двухэтапным процессом превращения аммония (NH+4) в нитриты (NО-2), а нитритов в нитраты (NO-3). Первый этап этого процесса (превращение аммония в нитриты) осуществляется автотрофными бактериями рода Nitrosomonas, которые в присутствии кислорода способны окислять аммоний до нитритов, используя в качестве источника энергии приблизительно 270 кДж/моль.
На втором этапе процесса нитрификации при окислении нитритов до нитратов выделяется примерно 73 кДж/моль. Эта реакция осуществляется бактериями рода Nitrobacter, которые используют выделяющуюся энергию на процессы обмена веществ.
Реакции превращения аммония в нитрит, а нитрита в нитрат требуют значительного количества кислорода. Стехиометрическая потребность в кислороде для превращения аммония в нитрит составляет 3,43 кг кислорода на 1 кг окисленного аммония. Превращение нитрита в нитрат требует 1,14 кг кислорода на 1 кг окисленного нитрита. Таким образом, превращение 1 кг аммония в нитрат требует 4,57 кг кислорода. Поскольку для работы биологического фильтра необходимо, по крайней мере, стехиометрическое количество кислорода, то поступление кислорода может стать фактором, ограничивающим нитрификационные процессы, протекающие в биофильтре.
Химические процессы превращения аммоний-нитрит-нитрат, используются бактериями Nifrosomonas и Nitrobacter для получения энергии. Бактерии утилизируют эту энергию, углекислый газ и кислород для продуцирования органических соединений, необходимых для роста клеток и обмена веществ. Объем массы клеток, образуемой растущими бактериями, имеет большое значение для биологических фильтров, поскольку отмирающие бактерии образуют взвешенные в воде частицы, которые закупоривают фильтр, что приводит к образованию в нем анаэробных участков, большим потерям напора протекающей через фильтр воды и другим нежелательным последствиям.
При окислении 1 кг аммония до нитрата образуется 147 г клеток Nitrosomonas и 20 г клеток Nitrobacter. К счастью, по сравнению с гетеротрофными бактериями нитрифицирующие бактерии продуцируют небольшую массу клеток на массу окисленного субстрата, и благодаря этому фильтры не так засоряются, если количество органических веществ, поступающих на нитрификационный фильтр, сведено к минимуму. Для реакции синтеза клеток автотрофных организмов участвует углекислый газ (С02). Углекислота частично обеспечивает потребность в кислороде, являясь также источником углерода.
Бактерия Nitrosomonas потребляет 3,02 кг кислорода на каждый килограмм аммония, окисленный до нитрита, a Nitrobacter—1,02 кг кислорода на килограмм нитрита, окисленный до нитрата. Таким образом, общее потребление кислорода составляет 4,04 кг на килограмм амоония, окисленный до нитрата. Однако, поскольку это отношение зависит от возраста культуры, количество кислорода, необходимое для полного окисления 1 кг аммония до нитрата, составляет от 4 до 4,6 кг.
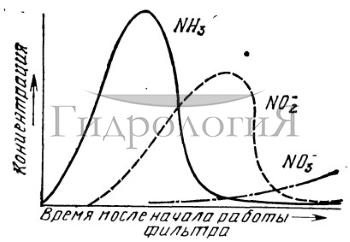
Рис. 2. Нитрификационные кривые.
На рис. 2 показана зависимость между содержанием аммиака, нитритов и нитратов на начальном этапе работы биологического фильтра. В начале работы популяция нитрифицирующих бактерий либо малочисленна, либо отсутствует вовсе, поэтому посадка рыбы в систему приведет к быстрому увеличению концентрации аммиака в воде. Этот момент является критическим, так как даже низкие концентрации аммиака могут оказаться губительными для культивируемых организмов. Снижение концентрации аммиака обычно сигнализирует о появлении жизнестойкой популяции Nitrosomonas, превращающей аммиак в нитриты. Однако такое предположение может привести к опасной самоуспокоенности. Обычно в биологическом фильтре присутствуют как гетеротрофные, так и автотрофные (нитрифицирующие) бактерии. Гетеротрофные бактерии характеризуются более ускоренным временем генерации (т. е. временем роста, размножения и продуцирования многочисленной популяции), чем автотрофные бактерии, - поэтому гетеротрофные бактерии, которые используют источник: простого органического углерода, но нуждаются в неорганическом азоте для обмена веществ, первоначально становятся доминирующими в фильтре и утилизируют продуцируемый в системе аммиак. Снижение содержания органического углерода подавляет рост гетеротрофных бактерий. Следовательно, первоначальное снижение концентрации аммиака может указывать не на нитрификацию, а на присутствие многочисленной популяции гетеротрофных бактерий. К счастью, это не часто наблюдается в аквакультуре.
Увеличение популяции Nitrosomonas приводит к возрастанию концентрации нитритов, которая достигает максимума, а затем начинает снижаться по мере роста популяции Nitrobacter, превращающей нитриты в нитраты. Увеличение концентрации нитритов также представляет опасность, так как они токсичны для рыб и многих других водных организмов. Систематический контроль за концентрацией нитритов и аммиака позволяет убедиться в том, что идет процесс нитрификации.
В любой водной системе аммиак присутствует в форме NH+4 и NH3, поскольку между этими двумя формами в воде существует равновесие. Неионная форма аммиака (NH3) токсична для большинства водных организмов в концентрациях 1 мг/л и ниже. Особенно чувствительны к NH3 лососи, на которых неблагоприятное воздействие оказывает длительное пребывание в воде с концентрацией NH3 0,006 мг/л. Равновесие между формами NH3 и NH+4 зависит от pH (рис. 3).

Рис. 3. Влияние pH и температуры на распределение аммиака и ионов аммония в воде
При pH менее 7 концентрация NH3 невелика и риск токсичности снижается. При более высоких значениях pH токсичность NH3 возрастает. Следует отметить, что в системах с соленой морской водой pH обычно составляет от 7,5 до 8,3, а в пресноводных — от 6,5 до 7,8.
В результате нитрификаций и синтеза бактерий образуются ионы водорода, поэтому во время нитрификации pH, как правило, снижается. В водных растворах ионы водорода нейтрализуются ионами бикарбоната (C02) в воде (при pH менее 8,5).
H+ + HCO-3 → CO2 + H2O
Конечным результатом этого процесса является снижение концентрации бикарбоната и увеличение содержания углекислоты, а оба эти условия способствуют снижению pH. На нейтрализацию ионов водорода, образующихся при окислении 1 кг аммония, идет примерно 7,13 кг бикарбоната в виде СаСОз. Расчеты с учетом равновесия угольной кислоты в пресной воде показывают, что если вся углекислота, образующаяся во время нейтрализации, остается в растворе, а pH должен быть выше 6,0, то количество аммония (в мг) на литр, которое может быть окислено, равно примерно 0,1 щелочности, выраженной в СаС03. Однако в большинстве замкнутых систем происходит частичное удаление углекислоты (например, в процессе аэрации), и обычно наблюдается некоторое снижение pH, поэтому правило «0,1 щелочности» дает консервативную оценку. Тем не менее для поддержания pH на необходимом уровне в воду с низкой щелочностью обычно необходимо добавлять карбонат или бикарбонат. Это часто осуществляется путем использования в качестве фильтрующего слоя карбонатных пород.
pH системы оказывает также непосредственное влияние на нитрифицирующие бактерии. По вопросу о влиянии pH на скорость окисления нитрифицирующими бактериями существуют различные мнения. В одних опытах наблюдали, что скорость окисления аммония неадаптированными культурами является постоянной только при pH 6,8—8. При pH ниже 6,8 скорость окисления аммония быстро уменьшается с понижением pH. Для pH выше 8 опыты не проводились. В других опытах наблюдали для Nitrosomonas europaea постоянную скорость окисления в диапазоне pH от 7,5 до 9, а для бактерий Nitrosomonas, только в диапазоне от 8,5 до 8,8. Все данные, за исключением последних, свидетельствуют о том, что, по-видимому, наибольшую и относительно постоянную скорость окисления бактерии Nitrosomonas имеют при pH от 7 до 9. Однако с течением времени фильтры могут акклимироваться к более низким значениям pH. Эксперементы показали, что через 10 дней после снижения pH до 6 бактериальная скорость окисления аммония до нитрита была равна скорости, наблюдавшейся в оптимальных пределах pH. Однако снижение pH до 5,5 создало условия, к которым нитрифицирующие бактерии не смогли адаптироваться даже с течением времени.
По вопросу о толерантности Nitrobacter, превращающих нитриты в нитраты, к колебаниям pH имеются следующие сведения: Nitrobacter осуществляют окисление с наибольшей скоростью только при pH от 8,4 до 9,2. Данные по очистке бытовых стоков показывают, что оптимальные скорости окисления наблюдались в области pH от 8,4 до 8,6. Опыт работы с нитрифицирующими фильтрами в рыбоводстве свидетельствует о том, что скорость превращения нитрита в нитрат достаточно высока для поддержания приемлемо низких концентраций нитрита при pH 6,5—8,5.
Температура также влияет на «скорость нитрификации в биологических фильтрах. С понижением температуры скорость реакции уменьшается.
При условии обеспечения стехиометрических потребностей в кислороде скорость нитрификации не зависит от концентрации кислорода. Однако при концентрациях кислорода ниже стехиометрических потребностей скорость реакции быстро уменьшается (рис. 4).

Рис. 4. Зависимость интенсивности нитрификации от стехиометрической потребности в кислороде.
По материалам: Уитон Ф. Техническое обеспечение аквакультуры.




